Uso de formulações lipídicas para aumentar a biodisponibilidade no desenvolvimento inicial

Quando uma molécula entra na Fase I, existem várias opções disponíveis para fazer uma formulação. A abordagem comumente usada é usar um API em uma formulação de garrafa ou cápsula. Estes são especialmente adequados para compostos que têm uma biodisponibilidade suficientemente alta e baixa variabilidade na farmacocinética (PK), pois é mais fácil conectar a formulação da Fase I com a formulação real do mercado usada nas fases posteriores. Se um composto tem variabilidade média e biodisponibilidade razoável, é possível usar uma abordagem já formulada que tem uma mistura de API na cápsula ou comprimido e cápsula mole. Isso depende, porém, das especificações da API e das opções disponíveis. Para APIs altamente potentes ou APIs de baixa dosagem, softgels podem ser uma boa solução, mas uma mistura de APIs em cápsulas ou comprimidos é comumente usada nos estágios iniciais.
Cerca de 70 por cento dos atuais canais de pesquisa incluem moléculas cada vez mais complexas que são difíceis de formular devido à alta variabilidade e / ou baixa biodisponibilidade. Essas características costumam ser a principal causa de falhas do produto. Para superar isso, os sistemas lipídicos têm sido usados historicamente para aproveitar os processos de digestão intrínseca dentro do trato GI para facilitar a absorção de APIs e melhorar a biodisponibilidade. Ainda assim, como não há uma única formulação “mágica” disponível que supere todos os desafios em relação à biodisponibilidade, as empresas devem rastrear várias opções de formulação para explorar qual oferece o melhor aprimoramento de biodisponibilidade.
Para evitar atrasos e problemas dispendiosos durante o desenvolvimento dessas moléculas, é importante entender quais mecanismos potenciais de absorção aumentada com formulações de lipídeos e ferramentas de triagem apropriadas estão disponíveis, bem como quais etapas subsequentes devem ser seguidas para aumento de escala e industrialização.
Os benefícios das formulações lipídicas
Existem vários aspectos fisiológicos do trato gastrointestinal onde os sistemas lipídicos podem interagir e ajudar a melhorar a biodisponibilidade. Quando uma formulação lipídica apropriadamente projetada entra no trato intestinal, o processo fisiológico do trato GI facilita a formação de uma microemulsão, ou seja, o tamanho das gotículas da formulação lipídica torna-se pequeno (intervalo nano). Isso aumenta a área de superfície da droga e seu potencial de absorção e solubilização. Além disso, uma vez que o fármaco é liberado do lipídeo para o lúmen intestinal, a solubilidade máxima do fármaco é alcançada, conduzindo a difusão através da membrana intestinal, melhorando assim a biodisponibilidade. E porque o API já está presente em um estado dissolvido na formulação de lipídios,
Muitos compostos BCS Classe II com baixa solubilidade podem se comportar de maneira diferente se ingeridos com alimentos, o que pode criar variações no perfil de PK que podem até levar a vários efeitos colaterais. As formulações lipídicas podem ajudar a reduzir ou superar o efeito alimentar. A formulação de lipídios também pode ajudar a contornar o metabolismo de primeira passagem, que é a ação do trato intestinal para realmente degradar ou metabolizar APIs pelo fígado (uma das formas naturais do corpo para realmente excretar os compostos) e, em vez disso, fazer uso do sistema de transporte linfático.
Um aspecto importante do transporte linfático é a lipofilicidade da molécula, que é tipicamente expressa como um logP ou um logP calculado (cLogP). A Figura 1 mostra os resultados de estudos destinados a examinar a partição de uma molécula em diferentes veículos lipídicos.
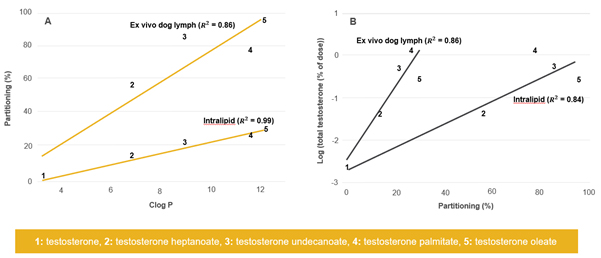
Figura 1: Previsão do transporte linfático; correlação com propriedades físicas e testes ex vivo 1
Os resultados mostram que se sua molécula tem um logP alto, a partição em veículos lipídicos é maior e a quantidade de dose absorvida também é maior. Portanto, se um logP for superior a quatro ou cinco, um sistema lipídico para melhorar a biodisponibilidade por meio do transporte linfático pode ser considerado. Embora os sistemas lipídicos ainda possam ser considerados para um composto com um logP abaixo de cinco devido ao comportamento da emulsificação ou à limitação da taxa de dissolução, é menos provável que ocorra o transporte linfático.
Os compostos BCS Classe II também podem ter taxa de dissolução limitada. Por exemplo, a velocidade na qual as moléculas entram em solubilidade é uma etapa limitante para a biodisponibilidade ou a solubilidade máxima do API no trato gastrointestinal é muito baixa para organizar trânsitos adequados para as membranas, evitando um aumento na biodisponibilidade. É crítico nos primeiros estágios de desenvolvimento entender se uma molécula tem uma limitação de solubilidade ou se ela tem uma limitação de taxa de dissolução. Felizmente, a formulação de lipídios pode funcionar em ambos os aspectos da formulação, já que o API é dissolvido no lipídio, aumentando a taxa de solubilidade, bem como melhorando a solubilidade máxima do API no lúmen gastrointestinal. Por essas razões, os sistemas lipídicos podem funcionar sem os dois fatores limitantes dos compostos BCS Classe II.
Selecionando e desenvolvendo formulações à base de lipídios
Quando se pensa em formulações lipídicas, a primeira coisa que vem à mente é a solução de óleo. No entanto, as formulações lipídicas oferecem uma ampla gama de opções. Eles podem ajudar a emulsificar em meio aquoso, podem ser formulados como semissólidos ou sólidos e também podem ser fabricados como suspensões. Normalmente, as formulações lipídicas são sólidas ou semissólidas à temperatura ambiente e tornam-se uma solução ou uma suspensão à temperatura corporal, ou seja, 37 graus Celsius. A seleção do tipo de formulação lipídica depende da solubilidade do API e da dose alvo. As formulações de lipídios também são particularmente adequadas para as diferentes fases (pré) -clínicas de desenvolvimento de produto desde o estágio inicial de desenvolvimento, normalmente usando quantidades muito pequenas de API. Isso é particularmente importante em projetos de Fase I, onde quantidades limitadas de material estão disponíveis ou a produção de grandes quantidades de API é muito cara. As formulações lipídicas podem ser desenvolvidas rapidamente e reunidas em uma variedade de dosagens em estudos de PK para animais.
As formulações lipídicas também podem ser administradas como líquidos, o que é benéfico em grupos selecionados de pacientes, como pediatria. Para aplicações clínicas e tamanho e finalidades comerciais, a melhor abordagem é encher a formulação em uma cápsula, onde as formulações de gel duro e mole podem ser usadas. Na verdade, a maioria das formulações à base de líquidos orais são comercializadas e fabricadas como cápsulas. Quando comparadas a outras formas de dosagem, como comprimidos ou secagem por pulverização, as cápsulas são mais fáceis de aumentar e mais econômicas. Por exemplo, ao observar os trens de equipamentos de fabricação de comprimidos, há pelo menos quatro etapas diferentes de aumento de escala para comprimidos, enquanto para cápsula mole apenas a preparação do medicamento requer aumento de escala do processo. Isso significa uma redução significativa no número de testes de fabricação, o que reduz custos e aumenta a velocidade de lançamento no mercado.
Como desenvolver uma formulação à base de lipídios
Geralmente, uma formulação à base de lipídios é iniciada por uma triagem de solubilidade, onde excipientes capazes de dissolver a dose necessária são identificados e uma avaliação preliminar da compatibilidade do API com os excipientes da triagem é fornecida. A próxima etapa é estabelecer a combinação certa e as concentrações de excipientes. Nesse estágio, é bom ter em mente as considerações sobre a adequação para encapsulamento, pois isso pode ser importante posteriormente, ao desenvolver as formas de dosagem iniciais, bem como para questões regulatórias, como segurança, toxicidade e pureza. Também evitará a necessidade de repetir o trabalho ou realizar testes adicionais no caminho.
Um teste de dispersão deve então ser concluído para avaliar as propriedades de emulsificação e dispersão de formulações de protótipo selecionadas. O teste de digestão de lipídios é feito nas formulações de melhor desempenho, em termos de propriedades de emulsificação e dispersão. Se as formulações tiverem um bom desempenho durante este teste de digestão de lipídios (ou seja, continuar a exibir uma alta solubilidade na fase de emulsão), esta é uma boa indicação de que também terão um bom desempenho durante os testes in vivo. Após este período, três a cinco formulações podem ser selecionadas e fabricadas para estudos de PK em animais. Todo o processo, desde as atividades de triagem inicial até a fabricação das amostras para estudos de caso, leva aproximadamente 12 semanas. Uma vez que as formulações tenham mostrado boa exposição em estudos de PK em animais, elas podem continuar imediatamente para o desenvolvimento da Fase I,
Estudo de caso: Formulação de um composto de classe II de BCS em um sistema de administração de medicamentos à base de lipídios
O objetivo deste projeto foi aumentar a solubilidade e biodisponibilidade do composto e, em última instância, estabelecer a relação entre o teste de lipólise in vitro e seu desempenho in vitro. O composto BCS Classe II tinha um peso molecular de aproximadamente 368 gramas por mol e um logP de quase seis, indicando uma boa possibilidade de ser solúvel em lipídios e uma formulação de lipídios teria sucesso. A formulação apresentou boa solubilidade em 15 diferentes excipientes, os quais foram selecionados por sua compatibilidade com cápsulas de gelatina sendo considerados para etapas posteriores. A tela de solubilidade é normalmente realizada em tubos Eppendorf, onde excipientes únicos são adicionados ao API e as amostras são primeiro equilibradas a 37 graus Celsius. Após 24 horas, eles são levados a 65 graus e, em seguida, de volta à temperatura ambiente,
Depois de identificar os excipientes nos quais a formulação era solúvel, a próxima etapa foi projetar as formulações de protótipo. Para auxiliar neste projeto, é utilizado o sistema de classificação da formulação lipídica. Esse sistema foi introduzido em 2000 e atualizado em 2006, quando o quarto tipo foi adicionado. A Figura 2 mostra as várias classes de sistemas lipídicos.
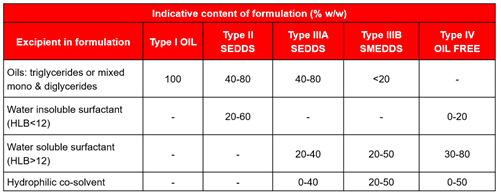
Figura 2: Sistema de classificação de formulação lipídica
Em resumo, existem quatro tipos de formulações, cada uma com características diferentes e, portanto, várias classes de excipientes:
- O tipo 1 é composto apenas de lipídios, ou seja, óleo, triglicerídeos ou mono e diglicerídeos mistos (sem uso de surfactantes).
- Tipo 2 são sistemas autoemulsificantes (lipídios usados em combinação com surfactantes insolúveis em água).
- O tipo 3 é dividido em duas subcategorias, mas também são emulsificantes. Uma mistura de óleos, surfactantes solúveis em água e, às vezes, co-surfactantes, também pode ser usada.
- O tipo 4 não usa óleos e geralmente é uma mistura de surfactantes e co-solventes solúveis em água.
O desenho da formulação lipídica é empírico e somente após o teste de dispersão e digestão lipídica é que se torna claro que tipo de formulação realizar enquanto in vivo. O medicamento foi formulado em vários sistemas contendo dois ou mais excipientes. É comum escolher misturas que representam os quatro tipos diferentes porque é muito cedo nesta fase para excluir certos tipos de formulações lipídicas.
O teste de dispersão é feito em um aparelho de dissolução modificado, primeiro com misturas de excipientes de placebo e depois com formulações ativas. O tempo de emulsificação, bem como a ausência de precipitação API após 30 minutos, são examinados. Normalmente, uma média de 20 a 30 misturas são testadas nesta fase. As quatro formulações de melhor desempenho (às vezes mais) são passadas para os locais de teste de lipólise de lipídios, onde a biodisponibilidade do API para testes clínicos é estimada. A Figura 3 é uma representação esquemática do teste de digestão de lipídios in vivo. A Figura 4 mostra os resultados para os quatro tipos diferentes de formulações (F1-F4) testados com o estudo de lipólise.
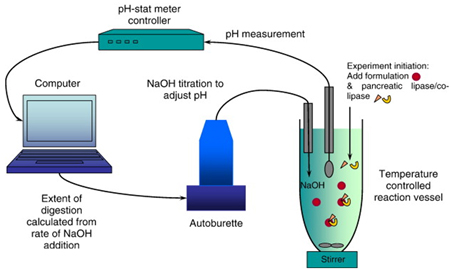
Figura 3: Configuração experimental para um experimento de digestão lipídica in vitro (adaptado de Porter et al., 2007)
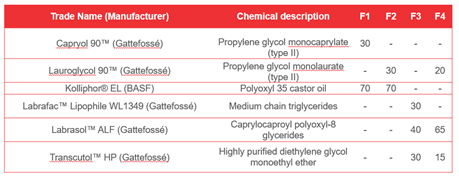
Figura 4: Triagem in vitro dos melhores conceitos de formulação do estágio 1
Após 60 minutos de lipólise, o fármaco recuperado no meio aquoso foi o mais alto para a formulação F2 com aproximadamente 40 por cento da dose incorporada sendo duas vezes maior do que o conteúdo do fármaco recuperado para as próximas formulações de melhor desempenho, que eram F1 e F4. O desempenho da formulação F3 foi considerado inferior a todas as outras, uma vez que apenas 10 por cento do fármaco foi recuperado após 60 minutos, levando à expectativa de que esta formulação teria um desempenho insatisfatório in vivo.
A perda na concentração versus o perfil de tempo após a administração oral mostra que a exposição foi significativamente maior quando o medicamento foi formulado com uma formulação à base de lipídios. O controle foi o pó API. As formulações F1 e F2 exibiram um tempo elevado para atingir as concentrações plasmáticas máximas, que foram mais curtas para F1, F4 e, especificamente, F2, mostrando uma propensão mais rápida dessas formulações para se dispersar no trato gastrointestinal e serem absorvidas. Mais importante ainda, a classificação dos resultados de biodisponibilidade relativa foi semelhante à classificação do fármaco recuperado em meio aquoso após o teste de lipólise in vitro de 60 minutos. Os resultados do estudo mostram o que podemos esperar dos testes de lipólise que são uma previsão da classificação na exposição e testes in vivo para diferentes formulações. Contudo,
O próximo passo no desenvolvimento de formulações baseadas em lipídios é o estudo de PK humana, onde a formulação vai diretamente para um estudo clínico humano ou através de uma otimização de formulação. Do lado clínico, o tempo é fundamental e, de fato, não há muito espaço para otimizar cada uma das misturas de excipientes selecionadas. Isso pode ser feito quando os estudos de PK em animais mostraram resultados promissores. Portanto, é aconselhável selecionar uma ou duas formulações de melhor desempenho e colocá-las em uma fase de otimização para solubilizar as propriedades de autoemulsificação do medicamento.
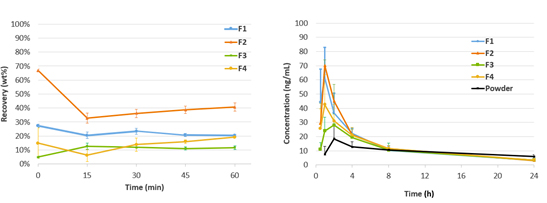
Figura 5: Triagem in vitro dos melhores conceitos de formulação dos estágios 1 e 2
Se o medicamento não se dissolver após uma variedade de excipientes serem testados e a solubilidade alvo com base na carga de medicamento alvo não puder ser determinada, as suspensões podem ser uma opção, particularmente quando o medicamento não se dissolve em lipídios. As suspensões lipídicas são essencialmente um fármaco cristalino disperso em um veículo lipídico. Eles podem fazer uso dos efeitos mediados pelo excipiente e da solubilização no intestino, e podem promover a permeação intestinal e / ou transporte linfático. Não se sabe muito neste estágio, porém, sobre como as suspensões de lipídios são absorvidas e processadas no trato gastrointestinal. Para o uso de uma formulação racional projetada para suspensões lipídicas, mais estudos são necessários para entender quais parâmetros podem contribuir para o sucesso dessas formulações in vivo.
Vários estudos têm demonstrado efeitos benéficos das suspensões lipídicas na biodisponibilidade e, possivelmente, redução da carga de excipientes sem afetar o desempenho in vivo. 2 Ao lado da suspensão lipídica, as formulações lipídicas alternativas que foram desenvolvidas nos últimos anos são as formulações lipídicas supersaturadas e supersaturáveis que demonstraram aumentar a carga do medicamento e também a biodisponibilidade do medicamento que inicialmente apresentava baixa solubilidade lipídica. 3
Conclusão
Uma parte significativa das novas entidades moleculares apresenta desafios com a biodisponibilidade durante os testes pré-clínicos e clínicos devido às limitações de solubilidade, e muitas delas são lipossolúveis. As formulações de lipídios podem ser muito úteis quando outras abordagens de formulação padrão não levam a uma melhoria suficiente na biodisponibilidade ou mostram grande variabilidade na exposição. Isso é particularmente verdadeiro para moléculas BCS Classe II, uma vez que muitas dessas moléculas apresentam biodisponibilidade aumentada quando ingeridas com alimentos. Os sistemas lipídicos também fazem uso de processos intrínsecos no trato gastrointestinal. No entanto, nenhuma formulação pode resolver todos os problemas de biodisponibilidade.
Determinar se um composto terá um desempenho melhor como uma formulação à base de lipídios deve ser feito caso a caso usando uma estratégia e projeto de triagem adequados. Como a formulação pode ser feita em laboratório com apenas alguns gramas de API, leva apenas 12 semanas para rastrear o desempenho da formulação. E embora a solubilidade de lipídios seja vital, o comportamento de emulsificação da formulação é o atributo de qualidade crítico mais relevante de uma formulação de lipídios. Na verdade, uma formulação com uma dose mais baixa pode apresentar maior biodisponibilidade do que uma formulação com uma dose mais alta. Assim, o projeto da formulação e uma boa previsão do comportamento in vivo são essenciais. Além das soluções lipídicas, as dispersões lipídicas e as formulações lipídicas supersaturáveis também podem melhorar a biodisponibilidade. No geral,
- Faassen, F. (2004). Aspectos biofarmacêuticos da administração oral de medicamentos . Tese de doutorado. Universidade de Utrecht, Holanda.
- Thomas N et al. (2014) AAPS J.
- Park, Heejun & Ha, Eun-Sol & Kim, Min-Soo. (2020). Status Atual dos Sistemas de Entrega de Medicamentos Auto-Emulsificantes Supersaturáveis. Farmacêutica. 12. 365. 10.3390 / pharmaceutics12040365
Nenhum comentário:
Postar um comentário