
Moléculas que são limitadas por um início de ação lento, um perfil de efeitos colaterais abaixo do ideal ou um processo de administração complicado, podem ser bons candidatos para adaptação a um formato de administração nasal de dose unitária ou bi-dose. Isto é especialmente verdadeiro para drogas direcionadas ao sistema nervoso central (SNC). Moléculas estabelecidas também podem se beneficiar de prazos de desenvolvimento mais curtos e ciclos de revisão regulatória.
A administração de spray nasal de medicamento oferece vantagens sobre a administração oral e intravenosa (IV). Andrew Samuelsson, Craig Davies-Cutting e Tom Clark, da Catalent, discutem as vantagens e oportunidades de adotar a tecnologia de aplicação nasal unitária e bi-dose.
Especialistas em destaque:
Andrew Samuelsson, Ph.D.
Gerente de Produto, Entrega Oral e Especializada
Craig Davies-Cutting, Ph.D.
Diretor, Produtos e Tecnologias Inalados
Tom Clark
Diretor, Operações Comerciais, Inalação
P: Quais são as vantagens da via nasal de administração?
SAMUELSSON: Historicamente, os sprays nasais têm sido tipicamente associados ao tratamento de condições locais, como alergias/rinites. No entanto, nos últimos 10 anos, houve um foco crescente na administração nasal para a entrega de moléculas ao SNC, bem como para a entrega sistêmica. A dosagem pela via intranasal mostrou um início de ação rápido, comparável ao da administração IV, com cinética consideravelmente mais rápida do que a administração oral 1-3 . A administração intranasal ganhou atenção como um método para atingir o SNC, uma vez que esta via fornece um meio prático e não invasivo de contornar a barreira hematoencefálica, alavancando a via nariz-cérebro putativa 4-7 .
Em relação à injeção intravenosa, a administração intranasal oferece um início de ação semelhante, sem o desconforto associado ou a necessidade de administração por um profissional de saúde. Ao atingir o SNC, a entrega intranasal pode atingir concentrações semelhantes de drogas no cérebro com uma concentração significativamente menor na circulação em relação a IV 3,8, provavelmente reduzindo a prevalência e gravidade dos efeitos colaterais sistêmicos observados com altas concentrações de drogas circulantes. Ao contrário das moléculas transportadas pela via nariz-cérebro, aquelas que vêm da circulação muitas vezes têm dificuldade em romper a barreira hematoencefálica, e estima-se que 98% dos medicamentos de pequenas moléculas não consigam passar por essa barreira 9. Técnicas que forçam o bypass (por exemplo, infusões intratecais) ou enfraquecem/abre a barreira hematoencefálica (por exemplo, injeção de manitol) podem acarretar riscos significativos 10,11 . Por fim, os sprays nasais evitam os riscos de ferimentos por picada de agulha e injeção, especialmente em situações em que o paciente não tem controle motor grosso (por exemplo, o paciente está tendo uma convulsão).
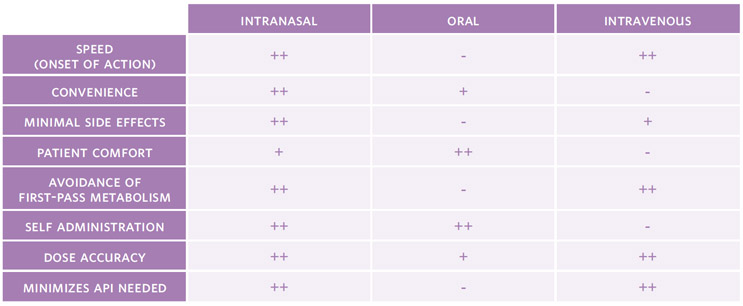
A administração oral é muitas vezes o formato preferido para autoadministração de drogas, mas sofre de metabolismo de primeira passagem, início de ação lento e muitos dos efeitos colaterais sistêmicos observados com IV. Doses mais altas são normalmente usadas para compensar o impacto do metabolismo hepático, que pode levar a desconforto ou toxicidade gastrointestinal e, em última análise, limitar o caminho de desenvolvimento de um medicamento oral. Embora uma porção de um spray nasal também termine no trato gastrointestinal, a concentração de uma droga administrada por via nasal é tipicamente ordens de magnitude menor do que a necessária para administração oral comparável, mitigando significativamente os riscos de efeitos colaterais 12 . Em geral, a administração intranasal pode superar vários desafios associados à administração oral e intravenosa, especialmente para condições do SNC (consulte a Tabela A).
O potencial de entrega do nariz ao cérebro como uma rota direcionada de entrega de drogas é grande; no entanto, existem alguns desafios, como um entendimento limitado da mucosa nasal 13 , evitar a imunogenicidade por meio de formulação otimizada 13e variabilidade de paciente para paciente na arquitetura ou obstrução da passagem nasal. Embora os efeitos colaterais sistêmicos e entéricos sejam geralmente menores com sprays nasais, os pacientes podem apresentar irritação na garganta, desconforto nasal e outros efeitos colaterais do nariz, garganta ou olhos1. Além disso, a via pode não funcionar para todos os tipos de moléculas, e os fabricantes e formuladores de dispositivos continuam procurando maneiras de maximizar o tempo de residência e absorção nos receptores olfativos e na mucosa nasal, respectivamente, e minimizar a depuração mucociliar no estômago.
Além do nariz ao cérebro, a administração intranasal também pode ser usada para administração sistêmica de drogas. A mucosa nasal é bem vascularizada e mais fina que a mucosa intestinal, permitindo a rápida absorção do fármaco diretamente na corrente sanguínea, contornando o metabolismo intestinal e hepático. Semelhante ao observado com o nariz ao cérebro, esta via permite um rápido início de ação, entrega não invasiva e o potencial para requisitos de dose mais baixos em relação ao necessário para administração oral. No entanto, em comparação com o IV, são necessárias doses mais altas e deve-se estar ciente do acúmulo potencial no cérebro através do caminho paralelo nariz-cérebro.
P: Como os sprays nasais de dose unitária ou bi-dose são diferentes dos sprays nasais multidose tradicionais? Quais são suas vantagens?
SAMUELSSON: Os sprays nasais de dose unitária e bi-dose são descartáveis e – comparados aos multidose – têm um perfil menor, são selados e menos propensos a vazar em uma bolsa ou mochila e não requerem primer antes do uso. Essas pequenas diferenças melhoram a conveniência e podem, em última análise, melhorar a adesão do paciente, especialmente para condições em que a necessidade de tratamento é pouco frequente a ponto de tornar impraticável transportar uma multidose maior.
Além disso, ao contrário dos sprays multidose, os sprays nasais de dose unitária geralmente podem ser livres de conservantes. Para produtos que contêm uma substância controlada, os dispositivos nasais de dose unitária e bi-dose limitam a capacidade de abuso devido ao uso de frascos selados com volumes definidos, baixas concentrações de drogas e formulações de drogas já destinadas à rápida absorção. Os dispositivos de dose unitária e bi-dose também fornecem volumes precisos de administração de medicamentos, reduzem os riscos de contaminação microbiana e são intrinsecamente invioláveis. Sem a necessidade de priming, eles também resultam em menos desperdício de API, tornando-os mais adequados para APIs caras.
P: Quais são as aplicações típicas dos dispositivos de aplicação nasal de dose unitária e bi-dose? Para que tipo de tratamentos são indicados?
DAVIES-CUTTING: Esses dispositivos nasais são boas opções para várias aplicações do SNC, incluindo doença de Parkinson, abuso de opióides, epilepsia/convulsões e aplicações de dor, como dor aguda/irruptiva, dor relacionada ao câncer, dor crônica e enxaqueca. Outras condições, como hipoglicemia relacionada ao diabetes e taquicardia superventricular paroxística, também são condições-alvo.
Os medicamentos atuais para essas condições, reformulados para administração intranasal, podem se beneficiar de maior velocidade de ação, entrega não invasiva ou perfil reduzido de efeitos colaterais e podem ser adaptados para administração nasal unitária ou bi-dose com prazos de desenvolvimento mais curtos e ciclos de revisão regulatória.
P: Quais são as diferenças entre dispositivos nasais de dose unitária e de dose dupla?
CLARK: As aplicações de dispositivos de dose unitária e bi-dose são basicamente as mesmas; a escolha entre dose unitária e dose dupla é determinada pelo volume necessário para administrar a dose necessária. Os dispositivos de dose unitária são adequados para administração de volumes de até 100μL e bi-dose para volumes de 100-200μL. Um produto de dose unitária normalmente tem um volume de preenchimento de 125μL para permitir a entrega de 100μL de formulação. Um aplicador de dose dupla tem um volume de preenchimento de 250μL para entrega de 200μL de formulação. A Catalent possui equipamentos de fabricação em escala comercial e clínica para formatos nasais de dose unitária e bi-dose.
P: A dose unitária é adequada apenas para líquidos?
CLARK: Não, também existem dispositivos de pó de dose unitária. De fato, o primeiro produto nasal em um dispositivo de pó de dose unitária foi recentemente aprovado e é fabricado pela Catalent.
Atualmente, a variante de pó seco só está disponível em formato de dose unitária, mas traz muitas das mesmas vantagens que a variante de dose unitária líquida, como formulação sem conservantes. As variantes em pó também podem administrar doses maiores e têm o potencial de serem mais estáveis do que suas contrapartes líquidas em cenários em que uma formulação líquida não fornece estabilidade adequada.
P: O que está impulsionando a mudança para o nasal unitário/bi-dose para fabricantes e clientes? Quais são algumas das tendências do setor?
CLARK: A mudança é em grande parte resultado dos benefícios mencionados acima para terapias agudas/SNC: um foco maior no controle da precisão da dose, entrega não invasiva e prevenção de abuso, especialmente à luz da epidemia de opióides. Os fabricantes de medicamentos também estão interessados nesse espaço, pois os sprays nasais de dose unitária e bi-dose são mais lucrativos do que os sprays multi-dose tradicionais. Atualmente, os produtos líquidos nasais compõem a maioria de todos os produtos para inalação em desenvolvimento, em grande parte impulsionados por vantagens farmacológicas e de fabricação, bem como um aumento nas vacinas administradas por via nasal.
P: Quais são as principais considerações para desenvolver um produto intranasal unitário/de dose dupla? E o desenvolvimento da formulação?
DAVIES-CUTTING: A cavidade nasal tem sido usada há muito tempo para entrega rápida e não invasiva. A chave para o desenvolvimento é garantir a entrega precisa e reproduzível, bem como a permeação eficaz do API através do epitélio nasal (por exemplo, usando intensificadores de permeação) ou prolongar o tempo de residência no receptor alvo ou na mucosa nasal em geral (por exemplo, com bioadesivos).
Para formulações de solução, há várias considerações importantes, incluindo: solubilidade do API, que pode afetar a dose potencial; estabilidade da solução; osmolaridade, que pode afetar a biodisponibilidade; pH, que pode afetar a solubilidade ou causar irritação; e enchimento da formulação (por exemplo, líquidos de microdosagem em pequenos frascos). Para o enchimento, a viscosidade é um fator crítico, pois não apenas afeta o enchimento do frasco e o desempenho da bomba de pulverização, mas também influencia o tempo de residência do medicamento no local de absorção.
Para formulações em pó, o fluxo de pó é uma questão importante para o enchimento de frascos pequenos (por exemplo, microdosagem). Além disso, a estabilidade física e as propriedades de tamanho, forma e superfície do pó são considerações importantes, pois todos esses elementos podem afetar a redispersão ou aerossolização do pó e, portanto, o desempenho de distribuição da dose.
P: Descreva as melhores práticas para estabelecer o perfil de produto alvo de qualidade desejado (QTPP).
DAVIES-CUTTING: Os sprays nasais são produtos de combinação de medicamentos e dispositivos e, portanto, exigem alinhamento com a seção do Código de Regulamentação Federal da FDA sobre regulamentação do sistema de qualidade (CFR820), que garante que os produtos de um fabricante atendam consistentemente aos requisitos e especificações aplicáveis. Para conseguir isso, é preciso considerar cuidadosamente a interação entre formulação, dispositivo e processo, pois todos esses são elementos críticos que controlam a qualidade do produto final da combinação droga-dispositivo.
O QTPP é um documento vivo, mas os principais elementos devem incluir:

P: Quais são os benefícios da qualidade por design (QbD) e como ela pode ser incorporada ao processo de desenvolvimento de produtos para dispositivos nasais unitários/de dose dupla?
DAVIES-CUTTING: Além de adotar o paradigma típico de desenvolvimento de produtos QbD descrito na ICH Q8(R2) para produtos farmacêuticos, há considerações adicionais para produtos de combinação de medicamentos e dispositivos que precisam ser abordados para garantir que o espaço de design tenha sido mapeado adequadamente e controlado.
Específicas para produtos combinados de dispositivos de spray nasal unitário/bi-dose, as principais questões de espaço de design são:
- O fornecedor da unidade/dispositivo binasal possui os controles apropriados (por exemplo, materiais, dimensões críticas, etc.)?
- Quais são os efeitos das tolerâncias de fabricação no desempenho de entrega do produto quando o dispositivo é casado com a formulação? (por exemplo, microdosagem da formulação no frasco do dispositivo, rolha do frasco e montagem do produto)
- Quais são os efeitos das tolerâncias do dispositivo na estabilidade do produto de combinação droga-dispositivo?
REFERÊNCIAS
- Bancke L, Dworak HA, Rodvold KA, Halvorsen MB, Gidal BE. Farmacocinética, farmacodinâmica e segurança de USL261, uma formulação de midazolam otimizada para administração intranasal, em um estudo randomizado com voluntários saudáveis. Epilepsia. 2015 novembro;56(11):1723-31.
- Fattinger K, Benowitz NL, Jones RT, Verotta D. Absorção da mucosa nasal versus gastrointestinal de cocaína administrada por via nasal. 2000 julho;56(4):305-10.
- Westin UE, Boström E, Gråsjö J, Hammarlund-Udenaes M, Björk E. Transferência direta do nariz para o cérebro de morfina após administração nasal a ratos. Farmácia Res. 2006 mar;23(3):565-72.
- Pardeshi CV, Belgamwa VS. Entrega direta de drogas do nariz ao cérebro por meio de vias nervosas integradas que contornam a barreira hematoencefálica: uma excelente plataforma para direcionamento do cérebro. Opinião do Especialista. Droga Entrega. 2013 jul;10(7):957-72.
- Kumar H, Mishra G, Sharam AK, Gothwa A, Kersharwani P, Gupta U. Intranasal Drug Delivery: Uma Abordagem Não Invasiva para a Melhor Entrega de Neuroterapêutica. Farmácia. Nanotechnol. 2017 maio; 3:203-214.
- Jiang Y, Li Y, Liu X. Parto intranasal: contornando a cortina de ferro para tratar distúrbios neurológicos. Opinião do Especialista. Droga Entrega. 2015 dez;(11):1717-25.
- Mittal D, Asgar A, Md S, Baboota, S, Sahni JK, Ali J. Insights sobre a entrega direta do nariz ao cérebro: Situação atual e perspectiva futura. Droga Entrega. 2014 mar;21(2):75-86.
- Wang Y, Aun R, Tse FL. Captação cerebral de diidroergotamina após administração intravenosa e nasal no rato. Biopharm Drug Dispos. 1998 Dez;19(9):571-5.
- Perdiz WM. A barreira hematoencefálica: gargalo no desenvolvimento de drogas cerebrais. NeuroRx. 2005 Jan;2(1):3-14.
- Joshi S, Meyers PM, Ornstein E. Intracarotid entrega de drogas: o potencial e as armadilhas. Anestesiologia. 2008 set;109(3):543-64.
- 11. Turner JA, Sears JM, Loeser JD. Sistemas programáveis de entrega intratecal de opióides para dor crônica não oncológica: uma revisão sistemática da eficácia e complicações. Clin J Dor. 2007 fev;23(2):180-95.
- Chen TC, Fonseca CO, Schonthal AH. Álcool perílico intranasal para terapia de glioma: mecanismos moleculares e desenvolvimento clínico. Int. J. de Mol. Sci. 2018 dez;19(12):3905.
- Gänger S, Schindowski K. Adaptando formulações para entrega intranasal do nariz ao cérebro: uma revisão sobre arquitetura, características físico-químicas e depuração mucociliar da mucosa olfativa nasal. Farmacêutica. 3 de agosto de 2018;10(3):116.
Nenhum comentário:
Postar um comentário