A “saga” da nitrosamina: lições aprendidas com cinco anos de escrutínio
Abstrato
O início da saga N – nitrosamina (NA) em 2018 foi principalmente relacionado a certos pequenos dialquil N-nitrosaminas provenientes da síntese do insumo farmacêutico ativo (API). No entanto, as avaliações abrangentes subsequentes realizadas em APIs, produtos farmacêuticos formulados e embalagens colocaram um tipo diferente de NAs no centro das atenções: uma gama diversificada de impurezas relacionadas a drogas e substâncias nitrosaminas complexas (NDSRIs). Eles podem se formar devido à presença de frações de amina secundária ou terciária potencialmente nitrosáveis em APIs ou impurezas API e agentes nitrosantes formados a partir de baixos níveis de nitrito presentes como impurezas. As propriedades únicas do grupo funcional amina o tornam insubstituível na síntese de APIs. Embora os níveis de nitrito possam ser reduzidos, a formação de NA em medicamentos não pode ser totalmente evitada,
Mesmo assim, espera-se que a exposição a NA por meio de produtos farmacêuticos seja de ordem de grandeza menor do que a exposição via alimentos ou formação endógena. Embora dados robustos de carcinogenicidade estejam disponíveis para muitos dos NAs pequenos e simples, há uma ausência distinta de tais dados para a maioria dos NDSRIs. Muitos grupos de trabalho foram, portanto, estabelecidos para compartilhar dados e melhorar rapidamente o conhecimento (seja em termos de dados de toxicidade, relações estrutura-atividade ou técnicas analíticas), para definir as melhores práticas para avaliar o potencial genotóxico de NDSRIs e avançar métodos para calcular IAs baseadas em fundamentos científicos sólidos. Em última análise, para proteger os pacientes do verdadeiro risco de câncer e garantir o acesso a medicamentos importantes, é crucial que os fabricantes e as autoridades de saúde se esforcem para implementar estratégias de controle de NA que sejam igualmente eficazes e realistas. Como a segurança do paciente é fundamental, a indústria farmacêutica está empenhada em garantir que os medicamentos que fornece sejam seguros e eficazes. Onde existem preocupações legítimas de segurança, é indiscutível que ações apropriadas devem ser tomadas, o que pode incluir a retirada de produtos do mercado.
1. Introdução
Já estamos no quinto ano da saga N-nitrosamina (NA), que tem sido uma preocupação crítica para fabricantes farmacêuticos e reguladores desde a primeira detecção de N-nitrosodimetilamina (NDMA) em valsartan em junho de 2018. NDMA e outros ANs pequenos e potentes permaneceram em foco, pois logo depois também foram encontrados em outros ingredientes farmacêuticos ativos sartan (APIs), (1,2) em piaglitazona e ranitidina (3,4) e em medicamentos à base de metformina. (5,6) A situação, no entanto, mudou drasticamente com o recall dos lotes de Chantix (vareniclina) nos EUA, Canadá e UE em meados de 2021 devido à presença da impureza relacionada à substância droga nitrosamina (NDSRI) nitrosovareniclina. (7,8) Isso foi rapidamente seguido por recalls de propranolol, (9) quinapril, (10) e orfenadrina (11) devido à presença de seus respectivos IRNDS (Figuras 1 e 2). Deve-se notar que esses recalls foram feitos com o pano de fundo de que não havia (e ainda há) acordo sobre como estabelecer ingestões aceitáveis
(AIs) para NDSRIs, com base em testes comparativos ou biológicos.
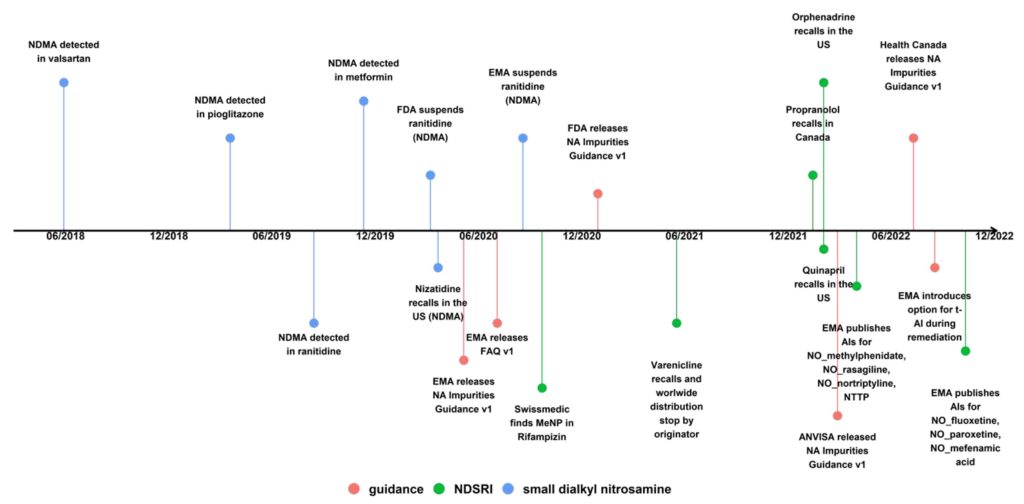
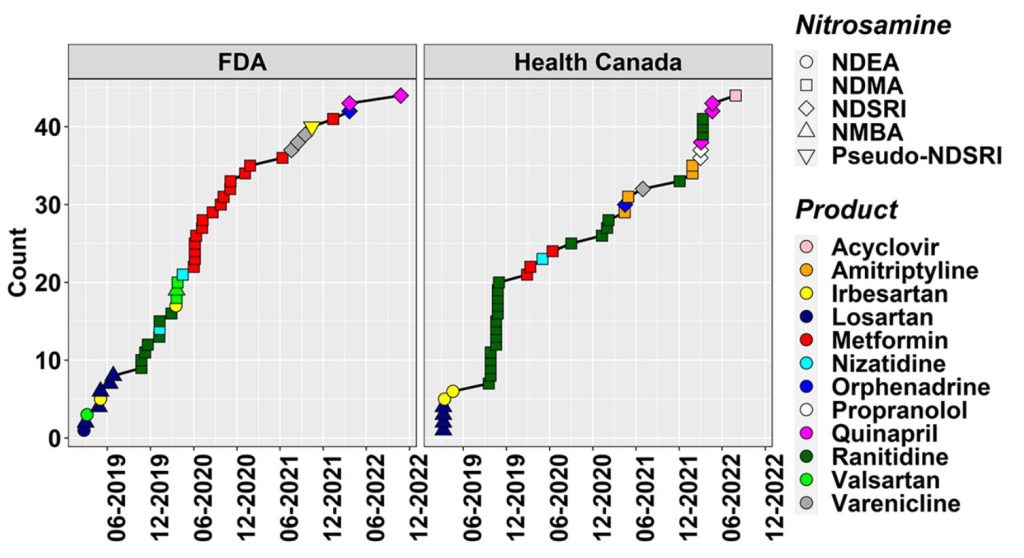
Embora haja literatura abrangente sobre a formação de NAs a partir de nitrito em solução (por exemplo, teste NAP), a formação de NDSRIs mesmo em produtos farmacêuticos sólidos (DPs) a partir de níveis de partes por milhão de nitrito foi surpreendente. Foi recentemente demonstrado que até 40% dos APIs comuns e 30% das impurezas dos APIs são potenciais precursores de NA, pois contêm porções de amina vulneráveis. Se apenas as aminas secundárias mais reativas forem consideradas, ainda 13-15% dos APIs estão potencialmente em risco. (12) Não é de surpreender que os NDSRIs tenham se tornado o foco tanto da perspectiva da indústria quanto da regulamentação.
A indústria e os reguladores estão agora na situação desafiadora de que os NDSRIs podem estar presentes em centenas, senão milhares de medicamentos, alguns deles afetando classes inteiras de medicamentos essenciais, como os β-bloqueadores. (12) Uma pesquisa realizada pela Medicines for Europe entre fabricantes farmacêuticos e apresentada na quarta reunião do EMA Nitrosamine Implementation Oversight Group (NIOG) com associações da indústria em 30 de novembro de 2022, revelou que até agora 90% dos possíveis NDSRIs identificados em NA avaliações de risco foram posteriormente confirmadas por testes analíticos.
Esta perspectiva visa colocar em perspectiva o risco potencial de produtos farmacêuticos contendo NA, lembrando-nos do que se sabe sobre NAs de alimentos, bem como da formação endógena de NA. Os NAs são formados a partir de aminas vulneráveis, então também discutimos por que eles não podem ser evitados e, consequentemente, por que os produtos farmacêuticos não podem ser completamente isentos de NA. Além disso, destacamos os desafios de sensibilidade analítica decorrentes do baixo padrão AI que é atualmente aplicado para alguns NAs e discutimos como AIs mais justificados cientificamente poderiam ser derivados usando comparativos. Isso também examina o potencial para o uso de AIs em combinação com correção para exposição menor que o tempo de vida e peso molecular. Diante disso, o valor dos testes de mutagenicidade in vitro (teste de Ames) e das iniciativas de compartilhamento de dados permanece alto. Finalmente,
2. Nitrosaminas dos Alimentos
Sabe-se há muitos anos que existe uma exposição humana substancial aos NAs dos alimentos. Uma revisão recente (13) destacou a publicação de 122 estudos de NA abrangendo uma variedade de ANs e suas fontes, uma proporção significativa dos quais relacionada a alimentos. A presença de NAs em alimentos também foi destacada em uma recente revisão de NAs pela EMA. (14) Com foco na literatura revisada por pares publicada antes de 2017, a revisão relatou que as classes de alimentos com o maior conteúdo total de NA (TNA) foram:
1. Gorduras, óleos e doces (TNA médio 8,9 ± 3,2 ng/g)
2. Carnes (TNA médio 8,1 ± 1,4 ng/g)
3. Peixe (TNA médio 5,6 ± 1,0 ng/g)
4. Legumes (TNA médio 5,4 ± 1,9 ng/g)
Dos NAs observados, o mais proeminente foi o NDMA (2,2 ± 0,3 ng/g), sugerindo uma carga diária superior a 2 μg/dia (com base em uma dieta de 2.000 calorias/dia composta de 500 g/dia de vegetais, 170 g/dia de gorduras, óleos e doces e 170 g/dia de carne). Uma exposição adicional de 1 μg/dia pode surgir do consumo típico de cerveja ou outras bebidas à base de malte.
Conforme destacado, o EFSA Panel on Contaminants in the Food Chain (CONTAM) lançou uma consulta pública sobre o projeto de parecer científico sobre os riscos para a saúde animal relacionados com a presença de AN nos alimentos. (14) Este documento apresentava uma avaliação da toxicidade dos NA, a exposição alimentar estimada dos cidadãos europeus aos NA cancerígenos presentes nos alimentos e, com base nestas, uma avaliação dos riscos para a saúde da população da UE. A EFSA avaliou 32 NAs e investigou sua presença em alimentos. Quantidades quantificáveis foram medidas apenas para um certo número de NAs. A caracterização do risco foi, portanto, limitada aos 10 NAs cancerígenos (TCNAs) que ocorrem nos alimentos (ou seja, NDMA, N-nitrosometiletilamina (NMEA), N-nitrosodietilamina (NDEA), N-nitrosodipropilamina (NDPA), N-nitrosodibutilamina (NDBA), N-nitrosometilanilina (NMA),
No total, foram avaliados 2.817 resultados de amostras de alimentos analisados de quatro países europeus entre 2003 e 2021 e, além disso, o painel CONTAM também examinou resultados de países da UE (n = 3.976) e países não pertencentes à UE (n = 27) extraídos de artigos publicados entre 1990 e 2021, selecionados com base em critérios de qualidade. Em comparação com a ref (13), a revisão da EFSA adotou uma abordagem ligeiramente diferente para a classificação das categorias de alimentos, definindo as cinco categorias de alimentos “Bebidas alcoólicas”, “Café, cacau, chá e infusões”, “Peixe, frutos do mar, anfíbios, répteis e invertebrados”, “Carnes e derivados” e “Temperos, molhos e condimentos”. Sua avaliação destacou que, em termos de avaliação da exposição alimentar, “Carne e produtos à base de carne” era a única categoria de alimentos para a qual havia dados disponíveis para todos os TCNAs individuais.
A correlação direta entre os dois estudos não é direta. Os resultados da revisão da EFSA mostraram que a exposição a TCNAs variou de 0 a 208,9 ng/kg de peso corporal/dia em pesquisas, faixas etárias e cenários, sendo “Carne e produtos à base de carne” a principal categoria de alimentos que contribui para a exposição a TCNA.
É interessante comparar os níveis de exposição de nitrosaminas da dieta e produtos farmacêuticos. Focando especificamente no NDMA, o limite para isso é definido como 96 ng/dia, com base em seu valor TD50. Este nível é 10 vezes menor do que o nível do potente mutagênico NDMA normalmente consumido em alimentos; isso sem sequer considerar o benefício associado aos produtos farmacêuticos.
É importante notar que outras fontes de ANs contribuem ainda mais para a exposição exógena, incluindo a exposição ocupacional. (15,16) De longe, o fator mais significativo é o uso de produtos de tabaco, que realmente supera todas as outras fontes de exposição, considerando que níveis acima de 20 μg/dia foram relatados. (13)
Baixe o artigo completo em PDF aqui: A “saga” da nitrosamina: lições aprendidas com cinco anos de escrutínio
ou leia aqui
The Nitrosamine “Saga”: Lessons Learned from Five Years of Scrutiny, Raphael Nudelman, Grace Kocks, Bruno Mouton, David J. Ponting, Joerg Schlingemann*, Stephanie Simon, Graham F. Smith, Andrew Teasdale e Anne-Laure Werner, Cite isto: Org. Processo Res. Dev. 2023, Data de publicação: 26 de julho de 2023, https://doi.org/10.1021/acs.oprd.3c00100, © 2023 Os autores. Publicado pela American Chemical Society
Nenhum comentário:
Postar um comentário